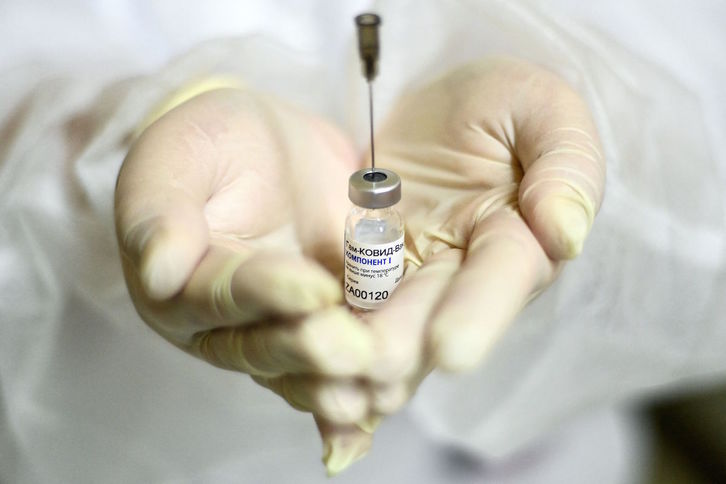
La Agencia Europea del Medicamento (EMA) ha comenzado este jueves un proceso de «revisión continua», un análisis en tiempo real, de los datos sobre la seguridad, la eficacia y la calidad de la vacuna rusa contra la covid-19 Sputnik-V, el proceso que podría conducir a autorizar el uso de este fármaco en la Unión Europea (UE).
En un comunicado, el regulador europeo ha informado de que la decisión de dar el paso «se basa en los resultados de los estudios de laboratorio y los estudios clínicos en adultos» que el desarrollador del fármaco ha compartido con los científicos europeos de la EMA, información que ya está siendo analizada por sus expertos en su sede de Ámsterdam.
Los estudios disponibles señalan que Sputnik V «desencadena la producción de anticuerpos y células inmunes que se dirigen al SARS-CoV-2» y pueden ayudar a proteger a las personas vacunadas contra la covid-19, algo que la EMA evaluará primero «con los estándares habituales de la UE en cuanto a eficacia, seguridad y calidad».
Según la EMA, fue un laboratorio alemán, R-Pharm Germany GmbH, el que presentó la solicitud para que la agencia estudie este antídoto, denominado «Gam-COVID-Vac», aunque la vacuna fue desarrollada por el Centro Nacional de Epidemiología y Microbiología Gamaleya de Rusia.
Esta revisión continuará hasta que haya suficiente información disponible para presentar una solicitud formal de autorización de comercialización en la UE, algo para lo que la EMA no tiene un calendario fijado todavía, aunque al iniciarse el análisis en tiempo real, «debería llevar menos tiempo de lo normal evaluar una eventual solicitud» para autorizar el fármaco, gracias al trabajo ya realizado durante la revisión continua.
Sputnik V se suma a las vacunas desarrolladas por el laboratorio alemán CureVac y el estadounidense Novavax, que también se encuentran en un proceso de evaluación continua de sus datos y aún no tiene fecha para solicitar una autorización de uso.
Moscú ofrece vacunar a 50 millones de europeos
Tras conocer la decisión de la EMA, el Fondo Ruso de Inversión Directa (RDIF, por sus siglas en inglés), desarrollador de la vacuna Sputnik V junto con el Centro Nacional de Epidemiología y Microbiología Gamaleya de Rusia, ha ofrecido a Bruselas la posibilidad de vacunar hasta a «50 millones de europeos a partir de junio de 2021» si finalmente el organismo europeo aprueba su vacuna.
«Tras la aprobación de la EMA, podríamos suministrar la vacuna a 50 millones de europeos a partir de junio de 2021», ha comentado a través de un comunicado el director general del RDIF, Kirill Dmitriev, quien ha aplaudido el inicio este jueves de una revisión continua de Sputnik V.
«Hemos proporcionado a la EMA datos exhaustivos sobre la vacuna rusa, cuyo uso ya está aprobado en más de 40 países. Sputnik V puede contribuir de forma importante a salvar millones de vidas en Europa y esperamos una revisión exhaustiva de los datos por parte de la EMA», ha apuntado Dmitriev.
En este sentido, ha defendido que «las asociaciones en materia de vacunas deben estar por encima de la política. La cooperación con la EMA es un ejemplo perfecto que demuestra que aunar esfuerzos es la única forma de acabar con la pandemia», ha reivindicado.
Varios Estados miembros de la UE han tomado decisiones unilaterales, al margen del bloque comunitario, para registrar Sputnik V sin la aprobación de la EMA, a pesar de que se acordó que el procedimiento sería homogéneo en la UE. De hecho, la vacuna ya está aprobada para su uso en Hungría y Eslovaquia. Hasta la fecha, 42 países con una población total de más de 1.100 millones de personas han autorizado Sputnik V.
«Sistema berria atera bitartean, polita litzateke berdin sentitzen garenon dimisioak pilatzea»

«Si a mi mujer le llega a patear un ultra habrían salido todos en tromba a condenar»

«Me hace mucha ilusión ver mi nombre en películas Disney junto a gente que admiro tanto»

Fallece Koldo Anza, hermano de Jon Anza y extrabajador de la Real