Proteinak eta beraien egitura
Teknologia atala irakurtzen ari zara, bai. Nahiz eta izenburuaren arabera, biologiaren atalean zaudela pentsatuko duzun. BBVA Fundazioako “Fronteras del conocimiento” sariak ikusita ere, oraingoan adimen artifizialaren inguruko saria topatu dugu, baina ez Informazioaren eta Komunikazioaren Teknologia arloan, Biologia eta Biomedikuntzan baizik.
Lehenengo eta behin utz iezadazue sari horien inguruko sarrera txiki bat egiten. BBVA Fundazioak Ikerketa Zientifikoen Kontseilu Gorenarekin lankidetzan emandako nazioarteko sari-multzoa dira, eta ikerketa zientifikoaren eta kultura-sorkuntzaren arloan egindako funtsezko ekarpenak aitortzen dituzte. Sari gazteak izan arren, 15 urte egin berri dituzte eta munduko sari entzutetsuenen artean tartea egitea lortu dute. Esate baterako, geroago Nobel sariren bat jaso dute BBVA Fundazioaren “Fronteras del conocimiento”ko 21 saridunek.
2022. urteko edizioan, eta aurten egindako sari-banaketan, Biologia eta Biomedikuntza atalean David Baker, Damis Hassabis eta John Micheal Jumper izan dira sarituak, adimen artifiziala erabiliz proteinen hiru dimentsioko egitura zehazki iragartzeko egindako ekarpenagatik.
Baina zergatik da garrantzitsua proteinen hiru dimentsioko egitura ezagutzea? Eta nola ematen da prozesu hori? Proteina baten egiturak bere funtzio biologikoa zehazten du. Proteinak oker tolestuz gero, degradatu egiten dira. Hortaz, proteina baten egitura ulertzea funtsezkoa da gaixotasunak ulertzeko, botikak diseinatzeko edo terapia gidatuak garatzeko. Proteinen azken konformazio hori (hiru dimentsioko egitura) da, oraindik ere, biologiako arazo garrantzitsuenetako bat.
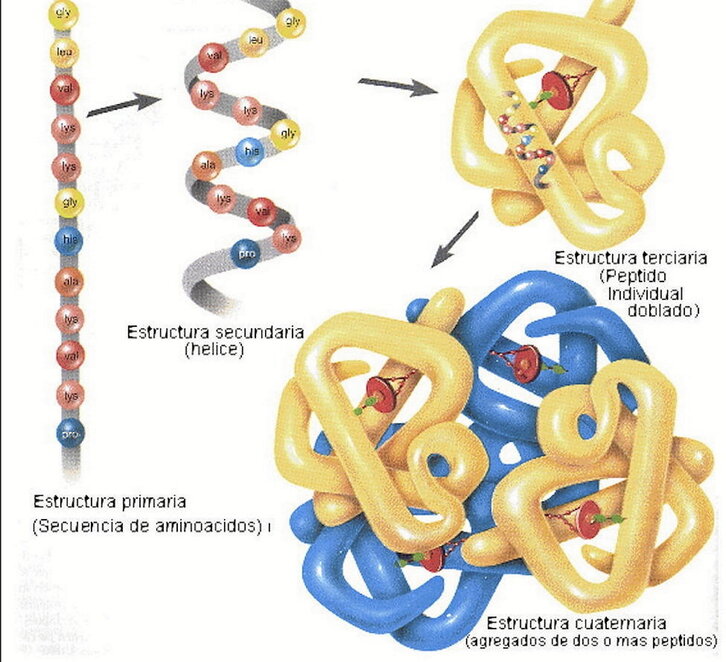
Aminoazidoen sekuentziak zehazten du toleste-bidea; aminoazidoz sortutako kate batetik abiatzen gara, eta horiek beraien arteko elkarrekintza sortzen dute, hiru dimentsioko egitura bilakatzeko. Lerro hauen azpian ageri den irudiak, hain zuzen ere, modu argian erakusten du aipatutako prozesua.
Saridunek adimen artifizialeko sistemak (RoseTTAFlod eta AlphaFold) sortu dituzte, aminoazido sekuentzia lineal batetik, proteinaren egitura aurreikusteko. Horretarako, neurona-sare sakonen ahalmen bete-beteaz probestu dira. Esperimentalki, laborategian urteak behar izaten dira proteina bakar baten egitura aurreikusteko. Baina ekarpen honi esker, aurreikuspena denbora laburrean (minututan) izateko gaitasuna lortu da.
Proteinen egitura denbora laburrean aurreikusteko gaitasunaz gain, iragarpenak zehatza ere izan behar du. CASP141-en (ikerketa-taldeek beren iragarpenen zehaztasun maila probatzeko erronka) antolatzaileek AlphaFold onartu zuten proteina-egituraren iragarpen-problemaren irtenbide gisa lortutako zehaztasun maila altuagatik. AlphaFold sistema erabiliz aurreikusten zen egitura esperimentalki lortutako egituren iragarpenaren berdina zen.
Ekarpen honi esker, zientzialariek proteinen arteko interakzioak aurreikusi, proteina guztiz berriak diseinatu eta diana farmakologiko berriak aurkitzeko gai dira. •
Aukeratu daitezkeen etiketen inguruan

Nafarroako Erresumako gotorleku bat Abadiñon, 791 metroko altitudean

«Ez nuen gure burua biktima bezala ikusi nahi, baizik eta borroka txikiak egin dituzten ama-alabak bezala»
Ekonomikaren markesa
